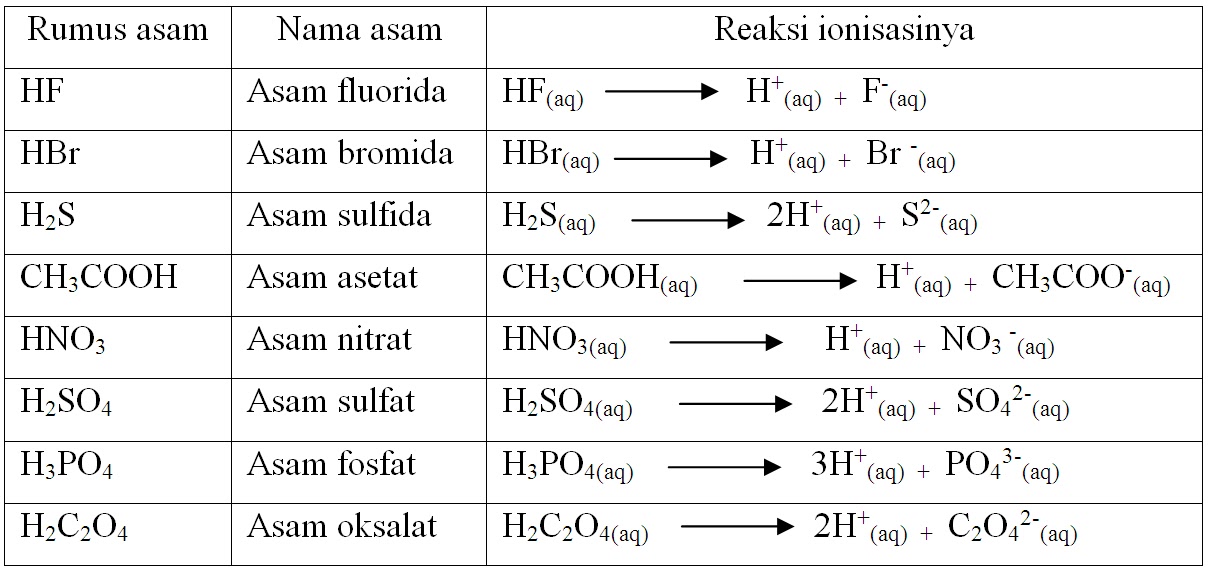
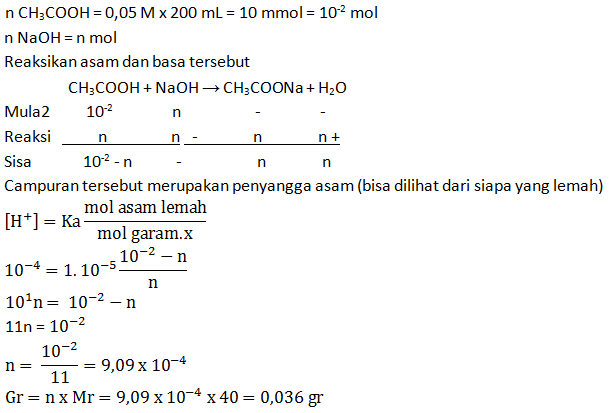H 2 so 3 0001 m jika k a 1 105. Contoh asam lemah adalah hf hcn hcooh dan lainnya.
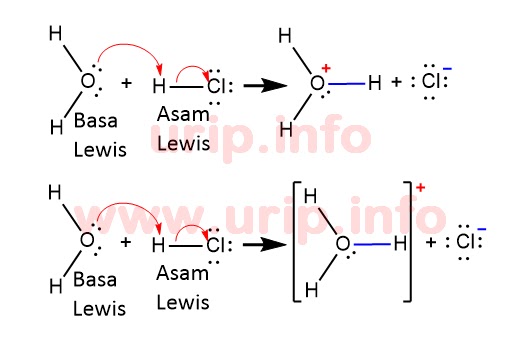
Reaksi Asam Basa Lewis Serta Penggolongannya Urip Dot Info
Contoh soal asam lemah. Ch 3 cooh 005 m jika derajat ionisasinya 1. Daftar asam basa kuat dan lemah january 19 2017 erika krissanta 6 comments asam basa calcium chemistry clorit hidro science karena lagi ngerjain tugas sekolah jadi sekalian aja ya nih erika kasih info tentang beberapa contoh asam dan basa sekaligus pembagiannya berdasarkan kuat dan lemahnya. Hcl hbr hi hno 3 hclo 4 h 2 so 4. Untuk memperdalam pengetahuanmu berikut materikimia berikan 10 contoh garam asam garam basa dan garam netral. Hno 3 01 m. Untuk lebih jelasnya dibawah ini diberikan beberapa contoh soal larutan asam basa yang disertai pembahasannya.
Jika ph larutan 001 m suatu asam lemah ha adalah 35 maka tetapan asam k a adalah. H 2 so 4 002 m. Cara menghitung ph larutan penyangga asam dan basa. Dengan demikian nilai k a dari asam kuat sangat besar. Oleh karena itu larutan garam dari asam lemah dan basa kuat akan meningkatkan konsentrasi oh dalam air sehingga larutannya bersifat basa ph 7. Sedangkan garam netral adalah garam yang terbentuk dari reaksi asam kuat dengan basa kuat dan juga dari reaksi asam lemah dengan basa lemah.
Contoh soal larutan asam basa. Van der waals forces and hydrogen bonds. Contoh soal asam basa pilihan ganda dan jawaban beserta pembahasan pada tahun 1923 g. Asam lemah dan basa lemah contoh basa lemah contoh soal asam lemah materi asam basa. September 19 2019 0. Asam adalah akseptor pasangan elektron.
Contoh soal asam kuat dan asam lemah 1 tentukan konsentrasi ion h dalam masing masing larutan berikut. 1 10 3 d. Garam seperti ch 3 coonh 4 yang dapat terbentuk dari reaksi asam lemah ch 3 cooh dan basa lemah nh 3 akan mengalami hidrolisis kation dan anionnya. Lewis mengemukakan teori asam basa yang lebih luas dibanding kedua teori sebelumnya dengan menekankan pada pasangan elektron yang berkaitan dengan struktur dan ikatanmenurut definisi asam basa lewis. Garam basa adalah garam yang terbentuk dari reaksi asam lemah dengan basa kuat. Basa adalah donor pasangan elektron.
1 10 7. Ph larutan garam demikian bergantung pada kekuatan. Untuk nilai k a yang sangat besar maka dapat dianggap bahwa asam terurai sempurna menjadi ion ionnya dan konsentrasi ion h dapat dihitung dari konsentrasi asam ha setimbang. Dalam air hampir seluruh asam kuat terurai menjadi ion ionnya sehingga derajat ionisasi α 1. Garam dari asam lemah dan basa lemah. Pengertian asam basa menurut brownsted lowry.
Hitunglah konsentrasi ion h 100 ml larutan hno 3 001 m.